Une étude conduite par :

1 • Procédures spécifiques à l'étude
1.1
Test de réactivité à la PEP pour orienter le traitement après la première randomisation
Les patients atteints d’un SDRA qui présentent les critères d’inclusion dans les 96 heures suivant leur admission en réanimation et dans les 72 heures suivant l’intubation seront randomisés dans l’un des trois groupes de la première randomisation. Dans l’heure qui suit la randomisation et avant l’activation de la stratégie de ventilation attribuée par la première randomisation, les patients subiront un test de réactivité à la PEP (PRT) qui comporte trois volets.
- Une période de ventilation de 20 minutes avec une PEP de 5 cmH2O.
Tout d’abord, immédiatement après leur inclusion, les patients seront évalués avec une PEP réglée à
5 cmH2O (il est possible d’évaluer les critères d’inclusion avec une PEP réglée à
5 cmH2O et accélérer ainsi l’inclusion dans l’étude). En bref, la PEP sera ajustée
pour atteindre une PEP totale de 5 cmH2O, le VT sera maintenu à 6 mL/kg IBW et les
autres paramètres ventilatoires resteront tels qu’ils étaient lors du test de sélection qui a permis
de qualifier le patient pour l’étude. La FiO2 peut être ajustée pour maintenir l’oxygénation
dans une fourchette acceptable. Après 20 minutes de ventilation avec une PEP réglée à 5 cmH2O,
la mécanique pulmonaire (PPLAT, ∆P, CRS) sera évaluée et des gaz du sang (GDS) artériels seront prélevés
pour calculer le rapport PaO2/FiO2 et évaluer la PaCO. En cas d’hypoxémie lorsque
la PEP est réglée à 5 cmH2O, la FiO2 sera augmentée afin de maintenir la SaO2
dans des limites acceptables. Si une hypoxémie sévère persiste malgré l’augmentation de la FiO2,
le test sera raccourci et interrompu immédiatement après le prélèvement des gaz artériels. - Une manœuvre de recrutement pulmonaire.
Ensuite, une manœuvre de recrutement pulmonaire sera effectuée en appliquant une minute de ventilation
contrôlée avec un VT réglé pour obtenir une pression inspiratoire de 45 cmH2O, une PEP de
15 cmH2O, une fréquence respiratoire de 10 respirations/min et un rapport I/E de 1:1.
Il n’y a pas de limite au VT pouvant être utilisé pour atteindre une PPLAT de 45 cmH2O.
Les périodes d’insufflation étant limitées à 3 secondes pour 10 respirations consécutives, cette manœuvre
est généralement bien tolérée du point de vue hémodynamique et peut entraîner une diminution limitée et
transitoire de la SpO2. Bien qu’il faille s’efforcer de maintenir ces réglages pendant une minute,
les investigateurs peuvent raccourcir la manœuvre après 30 secondes si une dégradation clinique significative
survient pendant la manœuvre. - Une période de ventilation de 20 minutes avec une PEP de 15 cmH2O.
La PEP restera ensuite réglée à 15 cmH2O, tandis que le VT sera réduit à 6 ml/kg IBW et
que les réglages de la fréquence respiratoire et du rapport inspiratoire/expiratoire seront ramenés aux
valeurs de base. Une analyse des GDS artériels sera effectuée après 20 minutes, sans autre modification
de la FiO2 ou de tout autre paramètre du ventilateur.
1.2
Première randomisation : stratégies de ventilation
Les stratégies de ventilation utilisées dans les 3 groupes de l’étude sont illustrées dans la figure 1.
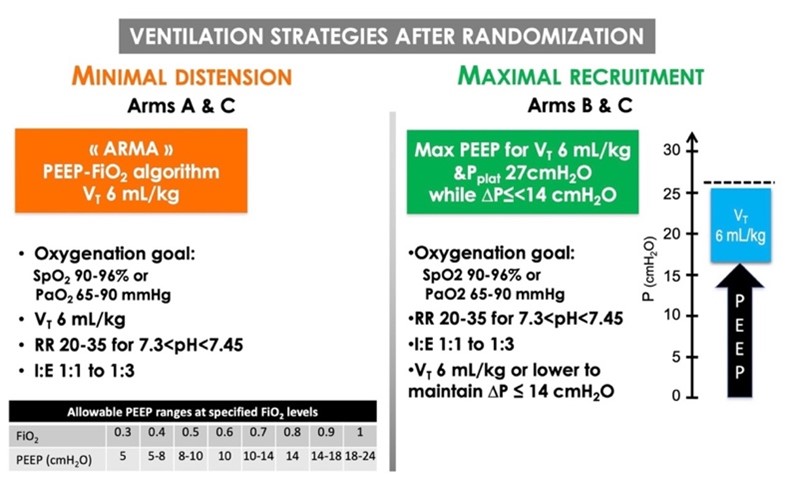
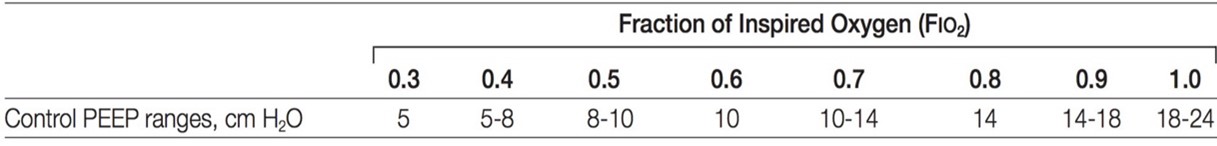
Cette stratégie de ventilation est légèrement adaptée du protocole ARDSnet utilisé dans les études ARMA et LOVS1,2. En bref, elle comprend une ventilation avec VT = 6 ml/kg IBW et PPLAT ≤ 30 cmH2O et un titrage combiné de la FiO2/PEP avec un tableau standardisé.
- Ajustement du volume courant : la ventilation assistée contrôlée (VAC) sera utilisée jusqu’à ce que les critères de sevrage soient remplis. Le volume courant sera fixé à 6 ml/kg IBW, calculé à partir du poids corporel prévu déterminé comme suit : IBW = X + 0,91 (taille en cm – 152,4), avec X = 50 pour les hommes et 45,5 pour les femmes. Le débit inspiratoire sera compris entre 50 et 70 L/min et la durée de la pause inspiratoire finale entre 0 et 0,5 s, et le rapport I:E sera maintenu entre 1:1 et 1:3. Tous les ventilateurs utilisés dans l’étude corrigeront les mesures du VT pour tenir compte de la compression des gaz. La mesure de PPLAT à l’aide d’une manœuvre d’occlusion télé-inspiratoire de 0,5 à 1 seconde sera effectuée pour confirmer que PPLAT est inférieure à 30 cmH2O. Si la PPLAT est > 30 cmH2O malgré un VT de 6 ml/kg IBW, la PEP sera réduite à un minimum de 5 cmH2O. Si PPLAT est > 32 cmH2O avec 6 ml/kg VT et 5 cmH2O PEEP, le VT sera réduit par paliers de 1 ml/kg jusqu’à 4 ml/kg, à condition que le pH reste ³ 7,15.
- Fréquence respiratoire et prise en charge de l’acidose : la fréquence respiratoire sera maintenue à 35/min maximum et ajustée pour obtenir des valeurs de PaCO2 telles que le pH artériel se situe entre 7,2 et 7,45. Lorsque le pH reste inférieur à 7,2 malgré une fréquence respiratoire de 35/min, le VT sera augmenté par paliers de 1 ml/kg jusqu’à 8 mL/kg jusqu’à ce que le pH soit ≥ 7,25, à condition que la PaCO2 soit ≥ 38 mm Hg et que la PPLAT < 32 cmH2O, si nécessaire en diminuant le niveau de PEP de 1 cmH2O par paliers jusqu’à un minimum de 5 cmH2O. Les stratégies détaillées de prise en charge de l’acidose respiratoire sévère sont décrites plus loin dans le manuel.
- Réglage de la FIO2 et des objectifs d’oxygénation : la FiO2 (0,21 à 1) sera réglée pour atteindre les objectifs d’oxygénation suivants : 90 % ≤ SpO2 ≤ 96 % ou 65 mmHg ≤ PaO2 ≤ 90 mmHg. Lorsque les mesures de PaO2 sont disponibles, elles auront priorité sur celles de la SpO2.
- Réglage de la PEP : la PEP sera réglée selon l’algorithme de protection pulmonaire ARMA (voir ci-dessous) en tenant compte de la PEP totale (somme de la PEP appliquée et de la PEP intrinsèque)1. Chez les patients complètement détendus ou sous blocage neuromusculaire, la PEP totale sera mesurée à l’aide de la méthode d’occlusion en fin d’expiration.
Afin de garantir une distension minimale et une séparation des niveaux de PEP dans les groupes étudiés, nous recommandons d’utiliser la PEP la plus basse possible dans la plage proposée pour une FiO2 donnée.
Comme pour la stratégie de distension minimale, les patients seront ventilés avec un VT initialement réglé à 6 ml/kg en VAC.
- Réglage de la PEP : La stratégie de réglage de la PEP est adaptée de l’essai Express3. Immédiatement après une manœuvre de recrutement effectuée comme décrit ci-dessus, la PEP sera ajustée en fonction de la pression des voies aériennes et sera maintenue aussi élevée que possible afin d’obtenir un VT égal à 6 mL/kg IBW sans augmenter la PPLAT au-dessus de 27 cmH2O — une valeur qui, selon plusieurs études, limite le risque de lésion pulmonaire liée à la distension. La mesure de la PPLAT à l’aide d’une manœuvre d’occlusion télé-inspiratoire de 0,5 à 1 seconde sera effectuée pour confirmer que PPLAT est ≤ 27 cmH2O. La PEP sera évaluée deux fois par jour et ajustée si nécessaire pour atteindre une PPLAT ≤ 27 cmH2O.
- Ajustement du volume courant pour limiter la ∆P : Après avoir réglé la PEP au niveau maximal pour une PPLAT de 27 cmH2O et un VT de 6 ml/kg, la pression motrice ∆P sera mesurée. Si ∆P dépasse 14 cmH2O, une réduction supplémentaire du VT sera effectuée par paliers de 0,5 mL/kg afin d’atteindre les objectifs de ventilation. En cas d’acidose sévère, la fréquence respiratoire sera augmentée jusqu’à un maximum de 35 rpm. La prise en charge de l’acidose respiratoire sévère est décrite plus loin dans le manuel.
- Fréquence respiratoire et prise en charge de l’acidose : La fréquence respiratoire sera maintenue à un maximum de 35/min et ajustée pour atteindre des valeurs de PaCO2 telles que le pH artériel se situe entre 7,2 et 7,45. Lorsque le pH reste inférieur à 7,2 malgré une fréquence respiratoire de 35/min, le VT sera augmenté par paliers de 1 ml/kg jusqu’à 8 ml/kg jusqu’à ce que le pH soit ≥ 7,25, à condition que la PaCO2 soit maintenue à ≥ 38 mm Hg et que la PPLAT < 32 cmH2O, si nécessaire en diminuant le niveau de PEP par paliers de 1 cmH2O jusqu’à un minimum de 5 cmH2O. Les stratégies détaillées de prise en charge de l’acidose respiratoire sévère sont décrites ci-dessous.
- Réglage de la FiO2 et des objectifs d’oxygénation : La FiO2 (0,21 à 1) sera réglée pour atteindre les objectifs d’oxygénation suivants : 90 % ≤ SpO2 ≤ 96 % ou 65 mmHg ≤ PaO2 ≤ 90 mmHg. Lorsque les mesures de PaO2 sont disponibles, elles auront priorité sur la SpO2.
1.3
Deuxième randomisation : utilisation du décubitus ventral (DV) et des curares
Dans le deuxième groupe d’interventions randomisées, le DV précoce et les curares seront utilisés dès que possible après la randomisation et au plus tard 6 heures après la dernière gazométrie artérielle admissible. Les curares sont utilisés pendant 48 heures, mais peuvent être arrêtés plus tôt si le rapport PaO2/FiO2 > 150 mmHg avec une PEP ≤ 12 cmH2O et une PPLAT ≤ 28 cmH2O pendant au moins 3 heures en décubitus dorsal.
-
Mise en place et posologie
Le personnel de l’étude s’assurera qu’un score RASS de -5 à -4 est atteint et documenté avant le début de la curarisation et que les patients sont en ventilation mécanique contrôlée. Le blocage neuromusculaire doit être initié dans les 6 heures suivant la randomisation dans le groupe avec utilisation précoce et systématique des curares. L’absence d’administration dans les 6 heures suivant la randomisation sera considérée comme un écart par rapport au protocole, mais le patient restera dans l’étude et dans l’analyse en intention de traiter.
Le cisatracurium sera le curare privilégié. Ce produit est couramment utilisé en France et a obtenu l’autorisation de l’EMEA. En ce qui concerne la dose, le cisatracurium sera administré au groupe interventionnel afin d’obtenir une réponse de 0 à 1 au train-of-four (TOF) réalisé au niveau du site orbiculaire (orbicularis oculi), ou aucune réponse (0/4) si le TOF est réalisé au niveau du site ulnaire (adducteur du pouce). Le TOF sera surveillé 1 heure après le début de la perfusion de curares et 1 heure après chaque changement de posologie. Une dose initiale de 0,25 mg/kg/heure de cisatracurium besylate peut être proposée, comme déjà décrit4. En cas de bloc neuromusculaire insuffisant (TOF supérieur aux objectifs), un bolus de 0,2 mg/kg et une augmentation de 20 % de la perfusion continue seront administrés4. En l’absence d’évaluation du TOF, le cisatracurium sera utilisé comme dans les études ACURASYS et ROSE (bolus de 15 mg de cisatracurium besylate, suivi d’une perfusion continue de 37,5 mg/heure)5,6.
-
Sédation
La posologie de sédatifs nécessaire pour obtenir un score RASS de -5 à -4 avant l’administration du cisatracurium doit être maintenue pendant la période de blocage neuromusculaire. Après la fin du blocage neuromusculaire ou en l’absence d’administration de curares, la sédation doit être adaptée afin de garantir la sécurité de la ventilation mécanique. Nous n’imposons aucun type ni aucune dose d’agents sédatifs.
-
Règles d’arrêt du blocage neuromusculaire
Au cours de la période d’intervention de 48 heures, le blocage peut être interrompu prématurément si le rapport PaO2/FiO2 > 150 mmHg à une PEP ≤ 12 cmH2O et une PPLAT ≤ 28 cmH2O et maintenu pendant au moins 3 heures alors que le patient est en décubitus dorsal. Si, après l’arrêt des curares, l’oxygénation se détériore de manière significative (PaO2/FiO2 < 120 mmHg), la curarisation doit être reprise. Après la période d’intervention de 48 heures, si l’oxygénation se détériore de manière significative (PaO2/FiO2 < 120 mmHg), le blocage neuromusculaire peut également être repris (décision du clinicien).
Dans ce groupe témoin pour la deuxième intervention, le décubitus ventral sera initié chez tous les patients présentant un PaO2/FiO2 < 150 mmHg après la deuxième randomisation. La sédation sera ajustée afin d’assurer une synchronisation patient-ventilateur cliniquement acceptable. Dans le groupe témoin, les curares ne seront utilisés qu’en tant que traitement de secours si PPLAT > 30 cmH2O pendant au moins 10 minutes malgré l’augmentation des doses de sédatifs, la diminution de VT (tout en maintenant un pH > 7,20) et une diminution de la PEP de 2 cmH2O (uniquement si pH ≤ 7,20) si tolérée5,6.
Nous encouragerons les sites à minimiser l’utilisation des curares dans le groupe témoin de la deuxième randomisation, pendant les 72 premières heures suivant l’inclusion et avant une éventuelle inclusion dans la deuxième partie du protocole principal. Nous encouragerons les interventions sans curarisation pour traiter les épisodes d’hypoxémie réfractaire, notamment en approfondissant la sédation.
-
Recommandation
Si la PPLAT reste supérieure à 30 cmH2O pendant au moins 10 minutes, il est recommandé d’administrer au patient des doses croissantes de sédatifs et de diminuer le VT ainsi que la PEP (pour atteindre une PPLAT de 30 cmH2O, uniquement si nécessaire et toléré) avant d’envisager l’utilisation du cisatracurium. Si réellement nécessaire, un bolus de 20 mg de cisatracurium est recommandé pour les patients randomisés dans le groupe « curares en traitement de secours ». Si cette injection intraveineuse rapide entraîne une diminution de la PPLAT ≥ 2 cmH2O, une deuxième injection de 20 mg de cisatracurium sera autorisée. Si, après l’injection, la pression plateau en fin d’inspiration ne diminue pas ou diminue de moins de 2 cmH2O, le cisatracurium ne doit pas être administré à nouveau pendant les 24 heures suivantes.
En cas d’asynchronie ou de dyssynchronie entre le patient et le ventilateur, il est recommandé d’adapter d’abord les réglages du ventilateur et, si nécessaire, d’utiliser des niveaux de sédation plus profonds. La perfusion de NMBAs n’est pas autorisée si la pression plateau est ≤ 30 cmH2O.
Si un curare est utilisé, il est recommandé de l’utiliser pendant la période la plus courte possible, avec une interruption minimale de la perfusion toutes les 24 heures, afin de ne pas prolonger le traitement plus longtemps que nécessaire.
-
Sédation
En l’absence de blocage neuromusculaire, comme dans l’étude ROSE5,6, la sédation est laissée à la discrétion du clinicien, mais il est recommandé d’utiliser un niveau de sédation suffisant pour assurer une synchronisation patient-ventilateur cliniquement acceptable lorsque le patient est dans un état grave, puis de viser un score RASS de 0 à -1 en l’absence de détresse respiratoire. Nous recommandons également des pauses quotidiennes dans la sédation s’il n’y a pas de contre-indication et de documenter les raisons de la sédation administrée pour un score RASS < -1.
2 • Soins cliniques des patients inclus
Bien que l’équipe soignante ait un contrôle total et indépendant sur la prise en charge des patients, les sites seront invités à respecter des recommandations de bonnes pratiques en matière de co-interventions pour minimiser les facteurs confondants pouvant survenir. Ces directives porteront notamment sur la gestion des fluides, les traitements médicamenteux concomitants (par exemple, la sédation…), les protocoles de sevrage, etc. D’une manière générale, ces directives s’appuient sur les recommandations d’experts concernant la prise en charge du SDRA et des patients en état de choc ou sous ventilation mécanique, ainsi que sur la dernière version des directives de la « Surviving Sepsis Campaign » 7-11.
2.1
Volume courant et mode de ventilation
Le volume courant est fixé à 6 mL/kg de poids corporel idéal (IBW) en utilisant le poids idéal théorique obtenu à l’aide de la formule suivante : P = X + 0,91 (taille en cm – 152,4), avec X = 50 pour les hommes et 45,5 pour les femmes. La ventilation assistée-contrôlée (VAC) est utilisée jusqu’à ce que les critères de sevrage soient remplis. Le débit inspiratoire est réglé entre 50 et 70 l/min. La durée de la pause télé-inspiratoire est réglée entre 0 et 0,5 seconde. Le ventilateur utilisé doit être équipé d’une compensation de mesure du volume pour la compliance du circuit (gaz compressible).
2.2
Objectifs d’oxygénation
La FiO2 (0,21 à 1) sera réglée pour atteindre les objectifs d’oxygénation suivants : 90 % ≤ SpO2 ≤96 % ou 65 mmHg ≤ PaO2 ≤90 mmHg. Lorsque les mesures de PaO2 sont disponibles, elles auront la priorité sur celles de SpO2 .
2.3
Humidification des gaz
Afin d’assurer une humidification adéquate pour tous les patients sous ventilation invasive tout en limitant l’espace mort instrumental, l’humidification des gaz inspirés sera de préférence réalisée à l’aide d’un humidificateur chauffant. Si un filtre à échange thermique et hygrométrique est utilisé, nous recommandons vivement d’utiliser un modèle à faible volume interne.
-
Systèmes acceptables :
- Humidificateur chauffant (de préférence) ou échangeur de chaleur et d’humidité (HME) selon la politique locale et l’équipement disponible.
-
Conseils pratiques :
- Préférez un humidificateur chauffant lorsque la rétention de CO2 est problématique (pour minimiser l’espace mort), en cas de sécrétions abondantes/épaisses, d’hypothermie, de ventilation prolongée ou de ventilation minute élevée.
- Remplacer le HME conformément aux instructions du fabricant ou plus tôt s’il est obstrué par des sécrétions ou si une résistance accrue est suspectée.
- Visez un conditionnement adéquat du gaz (généralement ~30 mg H2O/L d’humidité absolue près des voies respiratoires et un gaz inspiré chaud).
- Vérifiez toujours l’intégrité du circuit et la gestion de la condensation ; surveillez la résistance et l’alarme en cas d’occlusion du filtre.
2.4
Procédures d’aspiration
Nous recommandons d’effectuer les procédures d’aspiration selon les indications cliniques plutôt que de manière systématique. Afin d’éviter tout risque de dérecrutement alvéolaire induit par l’aspiration, l’aspiration trachéale sera effectuée sans déconnexion du ventilateur, soit à l’aide d’un système clos d’aspiration, soit à l’aide d’une sonde d’aspiration conventionnelle insérée à travers l’adaptateur pivotant du support de cathéter.
2.5
Sédation
Le choix des sédatifs et des analgésiques sera laissé à la discrétion du clinicien en charge. La profondeur de la sédation sera évaluée à l’aide du score RASS. Les doses de sédatifs et de narcotiques seront réévaluées au moins deux fois par jour et ajustées afin d’obtenir une fréquence respiratoire inférieure à 35/min, une bonne synchronisation patient-ventilateur et un score RASS cible suggéré dans le tableau ci-dessous.
Après le troisième jour, les investigateurs seront fortement encouragés à mettre en œuvre des protocoles de sédation ciblés sur le RASS afin de minimiser l’exposition à la sédation et à effectuer des arrêts quotidiens de la sédation.
| Situation clinique | Score RASS cible |
|---|---|
| Patients recevant des curares | -5 à -4 |
| Jour 0 à jour 3 suivant la dernière randomisation | -5 à -4 |
| Jour 4 et suivants | -3 à 0 |
| Patients ayant réussi le test de sevrage de la PEP et/ou ventilés avec une FiO2 ≤ 0,4 | -1 à 0 |
2.6
Curares
Pendant la période disponible avant la randomisation dans le cadre du PEPER, les cliniciens auront pour instruction d’éviter l’utilisation de curares et d’utiliser des doses plus élevées de sédatifs afin d’assurer la synchronisation entre le patient et le ventilateur. Si le patient a reçu une perfusion continue de curares (par exemple pendant le transfert préhospitalier ou interhospitalier), il est nécessaire d’arrêter la perfusion continue pour évaluer l’éligibilité du patient. L’administration en bolus de curares reste possible si elle est cliniquement indiquée malgré une sédation importante.
Pour les patients non randomisés pour la deuxième intervention de PEPER après expiration de la fenêtre de 72 heures, l’utilisation de curares sera autorisée chez les patients présentant un rapport PaO2/FiO2 <150 mmHg ou chez ceux qui répondent aux critères de secours PEPER pour les curares12. Le choix de du curare sera laissé à la discrétion du médecin traitant. Les investigateurs recevront pour instruction d’arrêter la curarisation 48 heures après son introduction. Les curares ne seront réintroduits que s’il s’avère impossible (malgré une optimisation de la sédation) d’obtenir les critères de bonne synchronisation patient-ventilateur décrits ci-dessous :
- Patient en mode VAC
- Fréquence respiratoire < 35 /min
- Pas de déformation majeure de la courbe pression-temps
- Absence ou rareté des asynchronies (double déclenchement ou effort gaspillé)
- Aucun signe de détresse respiratoire
En cas d’échec, il convient de tenter quotidiennement d’arrêter les curares.
Pour les patients randomisés dans le groupe « curares en secours » de l’étude PEPER, nous encouragerons vivement les sites à réduire au minimum l’utilisation des curares. Nous encouragerons les interventions sans curarisation pour traiter les épisodes d’hypoxémie réfractaire, notamment en approfondissant la sédation.
Recommandation : si la PPLAT reste supérieure à 30 cmH2O pendant au moins 10 minutes, il est recommandé d’administrer au patient des doses croissantes de sédatifs et de diminuer le VT avant d’envisager l’utilisation d’un curare. Si nécessaire, une injection intraveineuse de curares est recommandée. Si cette injection intraveineuse rapide entraîne une diminution de la PPLAT < 2 cmH2O, une deuxième injection de NMBA sera autorisée. Si, après l’injection, la PPLAT ne diminue pas ou diminue de moins de 2 cmH2O, les curares ne doivent pas être administrés à nouveau pendant les 24 heures suivantes. En cas d’asynchronie/dyssynchronie patient/ventilateur, il est recommandé d’adapter d’abord les réglages du ventilateur et, si nécessaire, d’utiliser des niveaux de sédation plus profonds. La perfusion de curares ne sera pas autorisée si la pression plateau est ≤ 30 cmH2O.
Si un curare est utilisé, il est recommandé de l’utiliser pendant la période la plus courte possible, avec une interruption minimale de la perfusion toutes les 24 heures, afin de ne pas prolonger le traitement plus longtemps que nécessaire.
2.7
Stratégie de sevrage
La stratégie globale de sevrage comprend : i) un essai de sevrage de la PEP, ii) une tentative d’établissement en toute sécurité de la ventilation spontanée, iii) si possible, un essai de respiration spontanée.
- Essai de sevrage de la PEP. À partir du troisième jour, un test de « sevrage de la PEP » doit être effectué une fois par jour chez tous les patients présentant un rapport PaO2/FiO2 > 200 mmHg avec une FiO2 < 0,6. En bref, la FiO2 sera réglée à 0,4 et la PEP sera progressivement réduite (sur 20 à 30 minutes) à 8 cmH2O en maintenant le VT constant. Si une désaturation persistante (SpO2 < 88 %, > 5 minutes) se produit au cours de cette manœuvre, les réglages précédents de la PEP et de la FiO2 seront rétablis. Si ce n’est pas le cas, les GDS artériels seront prélevés après 10 à 20 minutes de ventilation avec une PEP réglée à 8 cmH2O. Si le rapport PaO2/FiO2 ≥ 150 mmHg dans ces conditions (PEP = 8 cmH2O et FiO2 = 0,4), le patient sera considéré comme « pouvant être sevré de la PEP » et les chercheurs seront autorisés à diminuer la PEP selon la situation clinique. Si ce n’est pas le cas, les réglages précédents de la PEP et de la FiO2 seront rétablis.
- Tenter d’établir une respiration spontanée. La poursuite de la VM des patients « sevrables de la PEP » sera effectuée avec le mode de ventilation utilisé au moment de l’essai de sevrage de la PEP ou, de préférence, en utilisant une aide inspiratoire (PSV) avec un niveau de pression ajusté pour obtenir un VT < 8 mL/kg IBW, une pression inspiratoire < 30 cmH2O et une fréquence respiratoire inférieure à 35 respirations par minute avec une PEP ≤ 10 cmH2O et une FiO2 ≤ 0,4. En cas de désaturation prolongée (SpO2 < 88 %, > 15 min) dans ces conditions, les paramètres du mode de ventilation contrôlée seront rétablis conformément à la stratégie de ventilation attribuée définie après randomisation.
-
Essais de respiration spontanée.
Chez les patients qui tolèrent la PSV, les critères de sevrage seront recherchés chaque jour conformément aux recommandations standard et au protocole
en vigueur dans chaque centre13. Les essais de respiration spontanée seront réalisés à l’aide d’une pièce en T ou d’une assistance inspiratoire
à +7 cmH2O sans PEP (30 min – 2 h). L’essai sera répété une fois par jour jusqu’à l’extubation, tant que les critères de l’essai seront remplis.
L’extubation, ainsi que les décisions concernant la nécessité et le moment de la trachéotomie, seront laissées à la discrétion du médecin traitant.
Tous les patients qui réussissent le test de respiration sans assistance seront extubés ou autorisés à recevoir de l’oxygène sans pression positive via
une trachéotomie. Les patients qui nécessitent une ventilation invasive dans les 48 heures continueront à faire partie du ou des mêmes groupes d’étude.
Les patients présentant un risque élevé d’échec de l’extubation (c’est-à-dire âgés de plus de 65 ans ou souffrant d’une maladie cardiaque ou respiratoire chronique sous-jacente) recevront si possible une assistance respiratoire non invasive prophylactique, afin de prévenir une éventuelle insuffisance respiratoire aiguë post-extubation. Cette assistance peut prendre la forme d’une ventilation non invasive (VNI) (12 heures par jour pendant 2 jours, si possible), d’une oxygénothérapie nasale à haut débit (pendant 2 jours, si possible) ou d’une combinaison des deux. Pour tous les patients, les jours où l’oxygénothérapie nasale à haut débit est administrée seront considérés comme des jours sans ventilation si le patient ne présente pas de signes d’insuffisance respiratoire aiguë. Pour les patients sous VNI, les jours où la durée totale de la VNI est inférieure ou égale à 4 heures seront considérés comme des jours sans ventilation.
La respiration sans assistance est définie comme suit :- Extubation avec masque facial, oxygène par canule nasale ou air ambiant, OU
- Respiration avec tube en T, OU
- Respiration avec masque de trachéotomie, OU
- CPAP ≤ 5 cmH2O sans PS ou VNI intermittente pendant moins de 4 heures par jour ou oxygène nasal à haut débit.
2.8
Prise en charge de l’hypoxémie
Si la PaO2≥ 55 mmHg avec une FiO2 de 1,0 ne peut être maintenue malgré l’optimisation des paramètres ventilatoires selon la stratégie attribuée, les cliniciens peuvent recourir à d’autres traitements décrits dans les sections suivantes. Les procédures de secours seront choisies en fonction des pratiques en vigueur sur le site clinique et peuvent inclure la position ventrale, l’inhalation d’oxyde nitrique ou l’ECMO. Les participants continueront à être suivis et inclus dans l’analyse sur la base de l’intention de traiter. L’utilisation de procédures de secours constituera un résultat secondaire.
Tous les patients randomisés pour la deuxième intervention de l’essai PEPER (curares) devront être placés en DV dans les 6 heures suivant la deuxième randomisation.
Pour les patients qui ne répondaient pas aux critères de la deuxième intervention dans les 72 heures suivant la première randomisation, le DV sera le premier traitement à administrer en cas d’hypoxémie avant d’envisager toute autre stratégie complémentaire. Pour les patients inclus uniquement dans la première partie de l’essai PEPER (première randomisation), conformément aux recommandations des experts9, le DV sera mis en place en cas d’hypoxémie sévère définie par un rapport PaO2/FiO2 (mesuré avec une PEP ≥ 10 cmH2O) inférieur à 150 mmHg pendant plus de 12 heures, quel que soit le groupe de randomisation du patient. Dans l’ensemble, la technique utilisée sera adaptée du protocole PROSEVA14. Des séances d’au moins 16 heures consécutives doivent être effectuées. Des lits de réanimation standard seront utilisés pour tous les patients. Entre deux périodes de DV, les patients doivent être placés en position semi-assise. Une description détaillée de la procédure est proposée ci-dessous afin de garantir la standardisation du DV.
Le protocole de DV implique un repositionnement précis d’un patient sur le ventre, généralement sous sédation profonde, pour améliorer la fonction respiratoire, notamment en cas de détresse respiratoire aiguë (SDRA). La procédure nécessite une équipe coordonnée (idéalement, un minimum de 4-5 personnes formées sont nécessaires pour la manœuvre de retournement, y compris un kinésithérapeute ou un médecin pour gérer les voies respiratoires), une vérification des dispositifs médicaux, une protection des points de pression (visage, genoux) et une surveillance continue des fonctions vitales, du confort du patient et de la position des sondes. La position est maintenue pendant une durée d’au moins 16 h puis le patient est repositionné sur le dos.
-
Préparation
- Sécurité et environnement : reculer le lit du mur, enlever la tête de lit et rassembler tout le matériel nécessaire (draps, matériel de nettoyage, électrodes, etc.).
- Patient : la sédation profonde (curarisation selon randomisation) peut être nécessaire pour assurer le confort et l’efficacité du traitement. Vérifier l’intubation, les voies d’abord, et arrêter temporairement l’alimentation entérale.
- Matériel : s’assurer que les câbles, tubulures et perfusions ne soient pas enroulés autour du patient et que les machines soient positionnées de manière ergonomique.
-
Positionnement
- Protection des yeux : protéger les yeux du patient avant de commencer le déplacement pour éviter les lésions.
- Déplacement latéral : faire pivoter le patient sur le côté, en le déplaçant progressivement.
- Mise sur le ventre : placer le patient sur le ventre.
-
Ajustement et support :
- Positionner des coussins sous le thorax et le bassin pour soutenir et éviter la pression excessive sur le visage et le ventre.
- Placer un coussin sous les chevilles pour éviter les talons et décharger les points de pression.
- Faire pivoter la tête du patient pour la mettre en position neutre et protéger les yeux.
-
Surveillance post-positionnement
- Perméabilité des dispositifs : vérifier régulièrement la perméabilité de la sonde d’intubation ou de trachéotomie et des cathéters.
- Confort : surveiller la tolérance du patient et vérifier que les organes génitaux ne soient pas comprimés.
- Surveillance hémodynamique et respiratoire : surveiller les constantes hémodynamiques et respiratoires et ajuster la FiO2 en fonction de la SpO2 en respectant les instructions issues de la randomisation.
- Prévention des escarres : inspecter les points de pression et changer la position de la tête toutes les quatre heures pour éviter les escarres.
Le DV sera interrompu en cas de complication grave pendant la séance. Les complications entraînant l’interruption immédiate du DV comprennent l’extubation accidentelle, l’intubation sélective, l’obstruction du tube endotrachéal, l’hémoptysie, une SpO2 < 85 % ou une PaO2 < 55 mm Hg pendant plus de 5 minutes alors que la FiO2 est de 1, un arrêt cardiaque, une fréquence cardiaque inférieure à 30 battements par minute pendant plus d’une minute, une pression artérielle systolique < 60 mmHg pendant plus de 5 minutes et toute autre raison mettant la vie en danger pour laquelle le clinicien décide d’arrêter le traitement.
Une fois les patients placés en décubitus dorsal, la séance de DV peut être reprise à tout moment avant l’évaluation prévue après 4 heures en décubitus dorsal si les critères relatifs au niveau de SaO2, à la PaO2 ou aux deux sont remplis. Les critères pour ne pas recommencer le DV comprennent l’un des éléments suivants :
- une amélioration de l’oxygénation définie comme une PaO2/FiO2 ≥ 150 mmHg (en décubitus dorsal) avec des niveaux de PEP et de FiO2 indiqués par la stratégie de ventilation attribuée,
- une diminution du PaO2/FiO2 supérieure à 20 % pendant la séance pour 2 séances consécutives.
L’utilisation d’autres traitements de secours pour l’hypoxémie sévère, tels que le NO, le PGI2, l’almitrine ou l’ECMO, sera autorisée dans des conditions spécifiques.
Dans ce contexte, une hypoxémie sévère sera définie comme :
- la persistance d’un rapport PaO2/FiO2 < 150 mmHg pendant plus de 12 heures, ou
- la persistance d’un rapport PaO2/FiO2 < 100 mmHg pendant plus de 12 heures, avec une FiO2 > 0,8 et une PEP ≥ 15 cmH2O malgré l’utilisation du DV, quel que soit le groupe de randomisation du patient.
Chez ces patients, le DV tel que décrit ci-dessus sera le premier traitement de secours à mettre en œuvre avant d’envisager toute autre stratégie d’appoint. Dans l’ensemble, les cliniciens seront encouragés à suivre la stratégie définie dans les recommandations pour la prise en charge précoce du SDRA publiées par la SRLF9. Les indications des stratégies de secours seront soigneusement documentées dans le dossier médical du patient et dans l’eCRF.
D’autres traitements adjuvants, tels que l’inhalation de NO, peuvent être utilisés en cas d’hypoxémie réfractaire définie comme une PaO2/FiO2 < 70 mmHg pendant plus d’une heure avec une FiO2 > 0,8 malgré la mise en œuvre des niveaux de PEP indiqués par la stratégie ventilatoire après randomisation et le positionnement en décubitus ventral.
Si elles sont disponibles, ces stratégies doivent être essayées avant d’envisager le recours à l’ECMO veino-veineuse. Les modalités précises de ces traitements seront laissées à la discrétion du clinicien responsable. Leur nécessité doit être réévaluée au moins une fois par jour.
L’utilisation de l’oxygénation par membrane extracorporelle (ECMO) sera autorisée en cas d’hypoxémie réfractaire persistante malgré la position ventrale et l’inhalation de NO. L’ECMO pourrait probablement être envisagée chez les patients qui répondent aux critères d’inclusion d’EOLIA15 ou lorsque la ventilation mécanique devient dangereuse en raison d’une augmentation incontrôlée de la PPLAT :
- avec une PEP, un VT et une fréquence respiratoire réglés selon la stratégie attribuée après randomisation,
- malgré l’optimisation de la prise en charge du SDRA, y compris les curares, le DV et le NO inhalé.
La décision d’utiliser l’ECMO doit être évaluée en contact avec un centre expert. En cas d’utilisation de l’ECMO, le mode ventilatoire et les réglages du ventilateur seront laissés à la discrétion du clinicien en charge du patient.
Outre les manœuvres de recrutement décrites dans la description des procédures d’étude sur la PRT et l’initiation de la ventilation, les manœuvres de recrutement pulmonaire ne sont recommandées dans aucun des groupes de l’étude. Lorsqu’une évaluation au cas par cas indique qu’une telle manœuvre est utile ou indispensable chez un patient présentant une hypoxémie profonde, le médecin traitant pourra utiliser la manœuvre de recrutement pulmonaire de son choix. Nous recommandons de limiter la durée des manœuvres de recrutement à moins de 30 secondes en continu16.
Afin d’optimiser l’équilibre entre les risques potentiels (barotraumatisme et effets hémodynamiques) et les bénéfices (amélioration de la compliance pulmonaire et des échanges gazeux en présence d’un collapsus alvéolaire), seuls les patients qui présentent une amélioration des rapports PaO2/FiO2, de la compliance pulmonaire et de la PaCO2 bénéficieront d’une nouvelle manœuvre de recrutement si cela s’avère nécessaire pour améliorer l’oxygénation.
-
Si réponse favorable :
- Une nouvelle manœuvre de recrutement peut être réalisée si nécessaire pour améliorer l’oxygénation (selon évaluation clinique).
-
Si absence de réponse :
- Les patients qui ne présentent pas d’amélioration de la compliance pulmonaire statique (c’est-à-dire sans alvéoles recrutables) ne bénéficieront pas de manœuvres de recrutement supplémentaires.
- Ils ne recevront qu’un ajustement quotidien de la PEP.
Les indications et les résultats des manœuvres de recrutement seront soigneusement consignés dans le dossier médical du patient et dans l’eCRF.
2.9
Prise en charge de l’acidose, de la fréquence respiratoire et du VT
L’objectif est de maintenir le pH entre 7,2 et 7,45 (un pH à ~7,15 peut être accepté pendant de courtes périodes), avec une approche générale permettant une hypercapnie permissive si nécessaire pour respecter les objectifs de protection pulmonaire (VT, PPLAT et ∆P). Envisager le traitement de la composante métabolique de l’acidose si et lorsque cela est cliniquement indiqué (par exemple optimisation hémodynamique, hémodialyse pour acidose lactique sévère et lésion rénale aiguë, etc.).
-
Objectifs et actions :
- Augmenter la fréquence respiratoire jusqu’à 35/min par paliers de 2 rpm tout en évitant l’auto-PEP et en maintenant les limites de PPLAT.
- Réduire l’espace mort de l’appareil lorsque l’hypercapnie persiste (par exemple, retirer les supports/adaptateurs de cathéter, envisager de passer d’un HME à un humidificateur chauffant).
- Ajuster la sédation pour assurer une synchronisation adéquate entre le patient et le ventilateur.
- Le VT est augmenté progressivement jusqu’à 8 ml/kg par paliers de 1 ml/kg, à condition que la PaCO2 reste ≥ 38 mmHg et que PPLAT soit < 32 cmH2O.
- Réévaluer la situation après chaque modification (gaz du sang artériel, mécanique du ventilateur, hémodynamique).
- Si le pH reste < 7,2 malgré les modifications précédentes, diminuer les niveaux de PEP par paliers de 1 cmH2O jusqu’à un minimum de 5 cmH2O.
- Envisager l’administration de bicarbonate de sodium si le pH est < 7,15 avec répercussions hémodynamiques, après avoir minimisé l’espace mort et optimisé la ventilation comme décrit ci-dessus.
2.10
Autres ajustements ventilatoires
En cas d’asynchronie/dyssynchronie patient-ventilateur, il est recommandé d’abord d’adapter les réglages du ventilateur et, si nécessaire, d’utiliser des niveaux de sédation plus profonds.
La perfusion de curares n’est pas autorisée si PPLAT < 30 cmH2O.
- En l’absence d’effort inspiratoire, si PPLAT dépasse 30 cmH2O pendant au moins 10 minutes malgré l’augmentation des doses de sédatifs, le VT est diminué par paliers de 1 ml/kg toutes les 5 minutes tant que PPLAT > 30 cmH2O jusqu’à 4 ml/kg IBW si le pH reste > 7,20.
- Si cela est toléré, la PEP est diminuée de 2 cmH2O (pour les patients dont le pH est < 7,20).
-
Si nécessaire, un bolus de 20 mg de cisatracurium est recommandé pour les patients dans le groupe « curares en secours » de l’étude.
Si cette injection intraveineuse rapide entraîne une diminution de la PPLAT ≥ 2 cmH2O, une deuxième injection de 20 mg de cisatracurium
sera autorisée. Si, après l’injection, la PPLAT ne diminue pas ou diminue de moins de 2 cmH2O, le cisatracurium ne doit pas être administré
à nouveau pendant les 24 heures suivantes.
L’ECCO2R ou l’ECMO sont autorisés dans ce cas. Les centres qui utilisent systématiquement d’autres curares pour cette indication peuvent utiliser le rocuronium (dose bolus de 0,6 mg/kg) ou l’atracurium (0,5 mg/kg).
- Suivez les recommandations pour sevrer la PEP et la FiO2 selon le groupe de randomisation PEPER. Le test de sevrage de la PEP peut être effectué à partir du troisième jour chez tous les patients présentant un rapport PaO2/FiO2 > 200 mmHg avec une FiO2 < 0,6.
- Réduisez et arrêtez l’iNO s’il est utilisé.
- Essayer de sevrer l’ECMO si elle est utilisée.
En cas de pneumothorax (drainé ou non) ou de manifestations cliniques de barotraumatisme pendant l’étude, l’ajustement de la ventilation sera laissé au libre choix du clinicien tant que le pneumothorax et/ou le drain thoracique sont présents.
Tous les épisodes de barotraumatisme seront documentés et signalés comme des événements indésirables graves.
2.11
Prise en charge hémodynamique
La prise en charge hémodynamique sera laissée à la discrétion du médecin traitant. Comme cela est considéré comme une pratique standard pour le traitement du SDRA, tous les patients auront une ligne artérielle insérée. Nous recommandons que chez les patients atteints d’un SDRA sévère ou d’un SDRA associé à une septicémie qui ne répondent pas au traitement initial, une surveillance hémodynamique avancée (c’est-à-dire un cathéter artériel pulmonaire ou PiCCO) soit envisagée17. Une évaluation initiale de l’hémodynamique par échocardiographie est également recommandée.
Une précharge adéquate est un facteur déterminant pour l’optimisation de la PEP chez les patients atteints de SDRA présentant un fort potentiel de recrutement. Nous recommandons d’utiliser des indices dynamiques de précharge-dépendance pour détecter l’hypovolémie. En règle générale, et en l’absence d’hypovolémie manifeste, la tolérance hémodynamique à des niveaux élevés de PEP est assez bonne lorsque de petits VT sont utilisés. Si une diminution de la SaO2 se produit lorsque le niveau de PEP augmente, il convient de rechercher une hypovolémie et, si nécessaire, de procéder à une expansion volémique. Pour détecter l’hypovolémie chez le patient (en particulier au moment du passage à des niveaux de PEP plus élevés), les chercheurs seront encouragés à utiliser des indices dynamiques de réactivité liquidienne. Chez les patients présentant un CRS faible (<30 cmH2O) sous ventilation avec un VT faible, l’évaluation des variations de la pression différentielle et du débit systolique ne peut pas être utilisée de manière fiable comme test dynamique de la dépendance à la précharge. Nous proposons plutôt d’utiliser des tests d’occlusion en fin d’expiration pour évaluer la nécessité d’une charge liquidienne18.
Chez les patients ventilés avec une stratégie de recrutement maximal, lorsque le niveau initial de PEP est associé à une baisse de la pression artérielle moyenne supérieure à 20 % qui persiste malgré un bolus de 250 ml de cristalloïdes (éventuellement répété jusqu’à 1 000 ml) et un traitement intraveineux par catécholamines, le niveau de PEP peut être réduit de 2 cmH2O à un niveau ne pouvant être inférieur à 12 cmH2O. Une nouvelle tentative d’augmentation du niveau de PEP sera effectuée dans les 3 heures suivantes. En cas de désaturation persistante pendant l’augmentation du niveau de PEP, nous recommandons de rechercher un foramen ovale perméable par échographie transœsophagienne avec « test aux bulles » et de limiter le niveau de PEP à une valeur entraînant une pression plateau de 25-26 cmH2O.
En cas d’hypotension persistante ou de faible débit cardiaque malgré les mesures ci-dessus, nous recommandons de réaliser une échocardiographie afin de détecter la présence éventuelle d’un cœur pulmonaire aigu défini par la combinaison d’un rapport diamètre ventriculaire droit/gauche supérieur à 0,6 et d’un septum paradoxal. Cet examen peut être réalisé, selon le choix du médecin traitant, par voie transœsophagienne ou transthoracique. En cas de cœur pulmonaire aigu, la PEP sera réduite de 3-6 cmH2O sans descendre en dessous d’une valeur minimale de 5 cmH2O. Une nouvelle échocardiographie sera réalisée 2 heures après la mise en place du nouveau niveau de PEP. En cas de régression du cœur pulmonaire aigu, le niveau de PEP sera maintenu au niveau inférieur. Si ce n’est pas le cas, la PEP sera réinitialisée à sa valeur d’origine. Dans ce cas, l’utilisation éventuelle de NO inhalé sera laissée à la discrétion du clinicien responsable.
Chez les patients en choc septique, les investigateurs seront encouragés à suivre les directives relatives à la survie en cas de septicémie et i) à administrer 30 ml/kg de cristalloïdes au début de la réanimation, ii) à traiter les patients avec de la noradrénaline comme vasopresseur de choix afin de maintenir la PAM > 65 mmHg, iii) à traiter tous les patients sous noradrénaline (≥0,25 µg.kg-1.min-1) avec des stéroïdes (bolus intraveineux de 50 mg d’hydrocortisone toutes les 6 heures + comprimé de 50 μg de fludrocortisone).
La gestion des fluides pendant le choc ne sera pas limitée. Cependant, chez les patients qui ne sont pas en état de choc, une approche conservatrice en matière de fluides sera recommandée pour tous les patients participant à l’étude. Cette approche conservatrice de gestion des fluides sera appliquée à l’aide de l’algorithme ROSE6 .
2.12
Corticostéroïdes
Chez les patients sous ventilation mécanique prolongée et présentant une fibrose pulmonaire secondaire à l’évolution du SDRA, l’utilisation des corticostéroïdes19 reste controversée. Bien que l’administration d’un traitement corticostéroïde soit laissée à la discrétion du clinicien responsable, nous suggérons que l’utilisation de corticostéroïdes pour le SDRA ne soit envisagée que chez les patients présentant des marqueurs inflammatoires élevés, exempts d’infection et qui restent gravement hypoxémiques (PaO2/FiO2<150 mmHg avec FiO2 ≥0,8) et présentent une altération marquée de la compliance pulmonaire après le 14ème jour. L’utilisation de corticostéroïdes (quelle que soit l’indication, quelle que soit la molécule et quelle que soit la posologie) au cours des 5 premiers jours suivant la randomisation sera classée comme une utilisation précoce de corticostéroïdes, tandis que l’utilisation après 5 jours (quelle que soit l’indication, quelle que soit l’ e la molécule et quelle que soit la posologie) sera classée comme une utilisation tardive de corticostéroïdes.
2.13
Contrôle glycémique
Pour les deux études, une attention particulière sera accordée au contrôle de la glycémie. Chaque site utilisera ses propres normes de prise en charge, y compris les protocoles de perfusion d’insuline spécifiques à l’établissement, afin de maintenir la glycémie dans une fourchette cible de 80 à 180 mg/dl (4,4 à 10 mmol/l).
2.14
Dérogations au protocole
Tous les centres ont une grande expérience dans la prise en charge des patients atteints du SDRA. Chaque centre participant mettra tout en œuvre pour ne pas s’écarter des instructions fournies dans le protocole de l’étude et le manuel de l’investigateur. Toutefois, le clinicien responsable du patient peut, à tout moment, s’écarter de ces instructions s’il le juge nécessaire dans l’intérêt du patient. Il doit alors consigner cette décision et sa justification dans le dossier médical du patient et dans l’eCRF.
Références
- The ARDS Network. Ventilation avec des volumes courants plus faibles par rapport aux volumes courants traditionnels pour les lésions pulmonaires aiguës et le syndrome de détresse respiratoire aiguë. New Engl J Medicine 2000;342(18):1301-1308.
- Meade MO, Cook DJ, Guyatt GH, et al. Stratégie de ventilation utilisant de faibles volumes courants, des manœuvres de recrutement et une pression expiratoire positive élevée pour les lésions pulmonaires aiguës et le syndrome de détresse respiratoire aiguë : un essai contrôlé randomisé. Jama 2008;299(6):637-645.
- Mercat A, Richard J-CM, Vielle B, et al. Réglage de la pression expiratoire positive chez les adultes atteints d’une lésion pulmonaire aiguë et d’un syndrome de détresse respiratoire aiguë : essai contrôlé randomisé. Jama 2008;299(6):646-655.
- Hraiech S, Forel J-M, Guervilly C, et al. Comment réduire la consommation de cisatracurium chez les patients atteints du SDRA : l’étude TOF-ARDS. Ann Intensive Care 2017;7(1):79.
- Papazian L, Forel J-M, Gacouin A, et al. Les bloqueurs neuromusculaires dans le syndrome de détresse respiratoire aiguë précoce. New Engl J Medicine 2010;363(12):1107-1116.
- Network NH Lung, and Blood Institute PETAL Clinical Trials, Moss M, Huang DT, et al. Blocage neuromusculaire précoce dans le syndrome de détresse respiratoire aiguë. New Engl J Med 2019;380(21):1997-2008.
- Messina A, Matronola GM, Cecconi M. Optimisation et réduction individualisées des fluides chez les patients gravement malades en état de choc septique. Curr Opin Crit Care 2025;31(5):582–90.
- Dessap AM, AlShamsi F, Belletti A, et al. Recommandations cliniques 2025 de la Société européenne de médecine intensive (ESICM) sur la thérapie liquidienne chez les patients adultes gravement malades : partie 2 — le volume des liquides de réanimation. Intensiv Care Med 2025;51(3):461–77.
- Papazian L, Aubron C, Brochard L, et al. Lignes directrices officielles : prise en charge du syndrome de détresse respiratoire aiguë. Ann Intensive Care 2019;9(1):69.
- Fan E, Sorbo LD, Goligher EC, et al. Lignes directrices officielles de l’American Thoracic Society, de l’European Society of Intensive Care Medicine et de la Society of Critical Care Medicine : ventilation mécanique chez les patients adultes atteints du syndrome de détresse respiratoire aiguë. Am J Resp Crit Care 2017;195(9):1253-1263.
- Evans L, Rhodes A, Alhazzani W, et al. Campagne « Surviving sepsis » : directives internationales pour la prise en charge du sepsis et du choc septique 2021. Intens Care Med 2021;1-67.
- Papazian L, Hraiech S, Cazenave L, Forel J-M. Les agents bloquants neuromusculaires dans le cadre d’une stratégie de protection pulmonaire chez les patients atteints d’un SDRA sévère. Anaesth Crit Care Pa 2019;38(4):311–3.
- Perren A, Brochard L. Gestion des difficultés apparentes et cachées du sevrage de la ventilation mécanique. Intens Care Med 2013;39(11):1885-1895.
- Guérin C, Reignier J, Richard J-C, et al. Positionnement ventral dans le syndrome de détresse respiratoire aiguë sévère. New Engl J Medicine 2013;368(23):2159-2168.
- Combes A, Hajage D, Capellier G, et al. Oxygénation par membrane extracorporelle pour le syndrome de détresse respiratoire aiguë sévère. New Engl J Med 2018;378(21):1965-1975.
- Arnal J-M, Paquet J, Wysocki M, et al. Durée optimale d’une manœuvre de recrutement par inflation soutenue chez les patients atteints de SDRA. Intens Care Med 2011;37(10):1588-1594.
- Vieillard-Baron A, Matthay M, Teboul JL, et al. Opinion d’experts sur la prise en charge de l’hémodynamique chez les patients atteints de SDRA : focus sur les effets de la ventilation mécanique. Intens Care Med 2016;42(5):739-749.
- Silva S, Teboul J-L, Jozwiak M, Persichini R, Richard C, Monnet X. Le test d’occlusion en fin d’expiration prédit la réactivité à la précharge indépendamment de la pression expiratoire positive pendant le syndrome de détresse respiratoire aiguë. Crit Care Med 2013;41(7):1692-1701.
- Annane D, Pastores SM, Rochwerg B, et al. Lignes directrices pour le diagnostic et la prise en charge de l’insuffisance corticosurrénale liée à une maladie grave (CIRCI) chez les patients gravement malades (Partie I) : Society of Critical Care Medicine (SCCM) et European Society of Critical Care Medicine (ESICM) 2017. Crit Care Med 2017;45(12):1.